军用火箭燃料的类型
历史背景
火箭燃料包含燃料和氧化剂,并且与喷气燃料不同,它不需要外部成分:空气或水。 处于聚集状态的火箭燃料分为液体,固体和混合燃料。 液体燃料分为低温(组分的沸点低于零摄氏度)和高沸点(其余)。 固体燃料由化合物,固溶体或增塑成分组成。 混合燃料由处于不同聚集状态的组分组成;目前,它们处于研究阶段。

从历史上看,第一种火箭燃料是烟粉,它由硝酸盐(氧化剂),木炭(燃料)和硫(粘结剂)的混合物组成,最早在公元2世纪用于中国的火箭中。 带有固体推进剂火箭发动机(RDTT)的弹药在军事上用作燃烧和信号装置。

在19世纪末无烟火药的发明之后,开发了一种单组分弹道燃料,该燃料由硝化纤维素(燃料)在硝化甘油(氧化剂)中的固溶体组成。 弹道燃料与黑火药相比具有多种能量,具有较高的机械强度,结构良好,在储存过程中具有长期化学稳定性,成本较低。 这些品质预示了在装有固体推进剂火箭的火箭弹和手榴弹中最受欢迎的弹药中广泛使用弹道燃料。

20世纪上半叶,诸如气体动力学,燃烧物理学和高能化合物化学等科学学科的发展,使得通过使用液体成分来扩展火箭燃料的组成成为可能。 第一台Fau-2液体燃料火箭发动机军用火箭发动机使用了低温氧化剂-液态氧和高沸点燃料-乙醇。
第二次世界大战后的火箭 武器 与其他类型的武器相比,它在发展上享有优先地位,因为它能够在几公里(反应系统)到洲际射程(弹道导弹)任何距离向目标传送核弹。 此外,火箭武器在 航空,防空,地面部队和 舰队 由于使用火箭发动机发射弹药时缺乏后坐力。
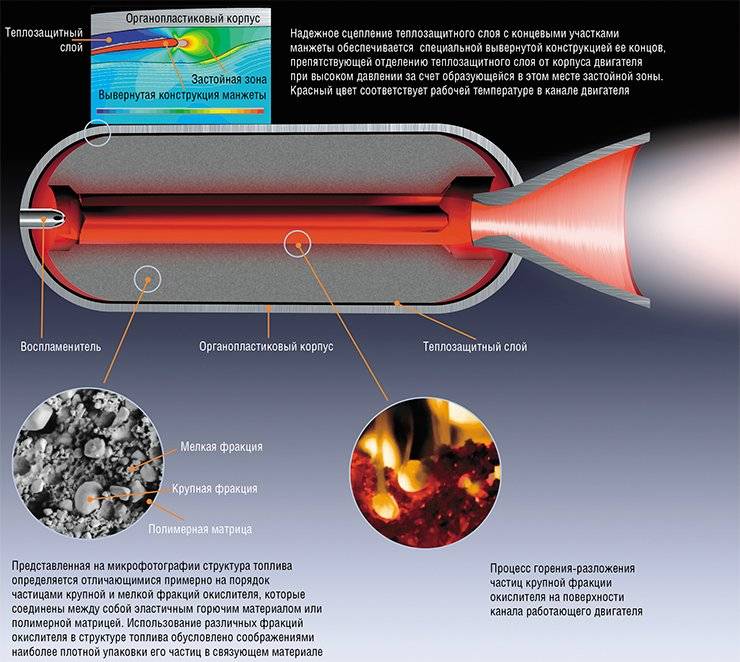
与弹道和液体火箭推进剂同时,多组分混合固体燃料由于其工作温度范围广,消除了部件溢出的危险,由于没有管道,阀门和燃料而降低了固体推进剂火箭发动机的成本,因此最适合军事用途。泵,每单位重量更大的牵引力。
火箭燃料的主要特征
除了其成分的聚集状态外,火箭燃料还具有以下指标:
-特定的推力脉冲;
-热稳定性;
-化学稳定性;
-生物毒性;
-密度;
-烟熏。
火箭燃料的比推力取决于发动机燃烧室中的压力和温度,以及燃烧产物的分子组成。 另外,特定的脉冲取决于发动机喷嘴的膨胀程度,但这更适用于火箭技术的外部环境(大气或外层空间)。
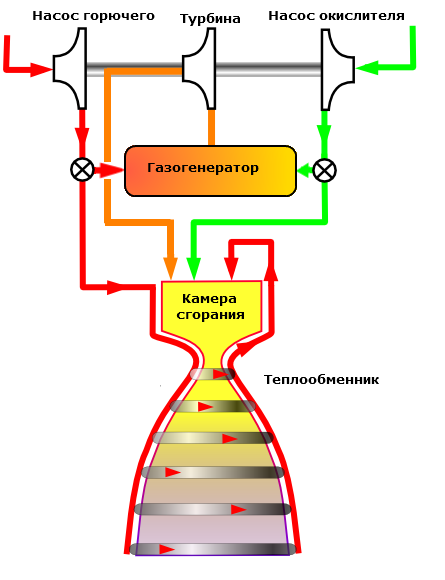
通过使用高强度的结构材料(用于火箭发动机的钢合金和用于固体推进火箭发动机的有机塑料)确保增加压力。 在这方面,由于与具有一个大燃烧室的固体燃料发动机壳体相比,液体推进火箭发动机的推进系统紧凑,因此液体推进火箭发动机领先于固体推进火箭发动机。
燃烧产物的高温是通过将铝金属添加到固体燃料或化合物氢化铝中来实现的。 液体燃料只有在用特殊添加剂增稠后才能使用。 火箭发动机的热保护通过燃料冷却来确保,固体推进剂火箭发动机的热保护通过将燃料块牢固地粘结到发动机壁上并在喷嘴关键部分使用可燃碳碳复合材料衬里来实现。

燃料燃烧/分解产物的分子组成会影响流量及其在喷嘴出口的聚集状态。 分子的重量越小,流速越大:最优选的燃烧产物是水分子,其次是氮气,二氧化碳,氯气和其他卤素氧化物。 最不优选的是氧化铝,其在发动机喷嘴中凝结成固态,从而减少膨胀气体的体积。 另外,由于最有效的带抛物线形表面的拉伐喷嘴的磨蚀,氧化铝部分迫使使用圆锥形喷嘴。
对于军用火箭燃料,由于火箭技术的工作温度范围广,其热稳定性尤为重要。 因此,低温液体燃料(氧气+煤油和氧气+氢气)仅在洲际弹道导弹(P-7和泰坦)发展的初期以及用于以下用途的太空火箭发射器(航天飞机和能源)中使用向地球轨道发射卫星和太空武器。
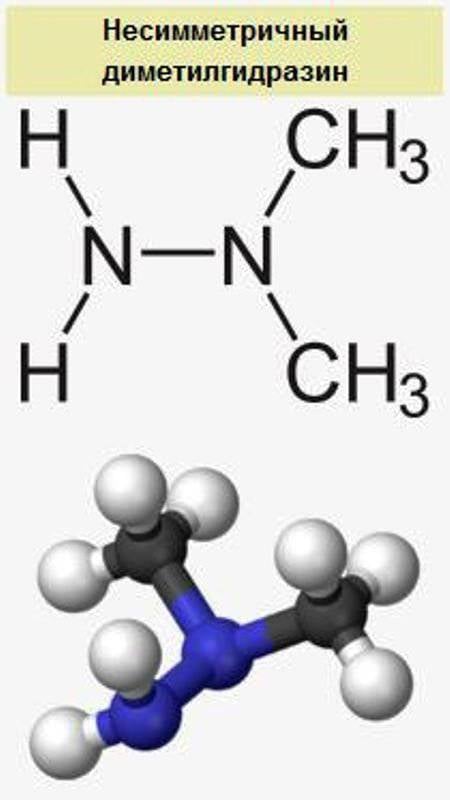
当前,军事部门仅使用基于四氧化氮(AT,一种氧化剂)和不对称二甲基肼(UDMH,一种燃料)的高沸点液体燃料。 该燃料对的热稳定性由AT(+ 21°C)的沸点确定,这限制了ICBMs和SLBMs导弹筒仓处于恒温状态的导弹对这种燃料的使用。 由于部件的侵略性,世界上只有一个国家拥有/拥有用于生产和操作导弹坦克的技术-苏联/ RF(Voevoda和Sarmat ICBM,Sineva和Liner SLBM)。 作为例外,AT + UDMH被用作X-22 Storm巡航导弹的燃料,但是由于地面操作方面的问题,X-22及其下一代X-32计划由使用喷气发动机的Zircon巡航导弹取代,煤油作为燃料。
固体燃料的热稳定性主要取决于溶剂和聚合物粘合剂的相应性能。 在弹道燃料的成分中,溶剂为硝酸甘油,在与硝酸纤维素的固溶体中,其工作温度范围为负50°C。 在混合燃料中,使用具有相同工作温度范围的各种合成橡胶作为聚合物粘合剂。 但是,固体燃料主要成分的热稳定性(二硝酰胺铵+ 97°C,氢化铝+ 105°C,硝化纤维+ 160°C,高氯酸铵和辛酸+ 200°C)大大超过了已知粘合剂的相似性能,因此具有重要意义。寻找他们的新化合物。
化学上最稳定的燃料对是AT + UDMH,因为它开发了一种独特的家用技术,可以在略微超出氮气压力的情况下在铝罐中进行无限制的长时间储存。 由于聚合物及其技术溶剂的自发分解,所有固体燃料都会随着时间的推移而化学降解,然后低聚物会与其他更稳定的燃料组分发生化学反应。 因此,固体推进剂检查仪需要定期更换。
火箭燃料的生物毒性成分是UDMH,它会影响中枢神经系统,人的眼睛粘膜和消化道,并引发癌症。 在这方面,使用自给式呼吸器在化学防护隔热服中使用UDMH。
燃料的密度值直接影响火箭发动机和固体推进剂火箭船体的燃料箱质量:密度越高,火箭的寄生质量越低。 氢+氧燃料对的最低密度为0,34 g / cu。 厘米,对于一对煤油+氧气,密度为1,09 g / cu。 厘米,AT + UDMH-1,19克/立方米。 厘米,硝酸纤维素+硝酸甘油-1,62克/立方米。 厘米,铝/氢化铝+高氯酸铵/二硝酰胺-1,7 g / cc,八价+高氯酸铵-1,9 g / cc 应当牢记的是,轴向燃烧固体推进剂的固体燃料密度约为燃料密度的一半,这是由于燃烧通道的星形截面用于保持燃烧室中的恒定压力而与燃料的燃烧程度无关。 弹道燃料也是如此,其以一组带状或方格的形式形成,以减少火箭和火箭的燃烧时间和加速距离。 与它们相反,基于HMX的固体推进剂固体推进剂固体推进剂固体燃料中的装料密度与为其指示的最大密度一致。
火箭燃料的最后一个主要特征是燃烧产物的烟雾,从视觉上掩盖了火箭和火箭的飞行。 该特征在包含铝的固体燃料中是固有的,该铝的氧化物在火箭发动机的喷嘴中膨胀期间会凝结成固态。 因此,这些燃料用于固体火箭推进弹道导弹,其弹道的有效部分在敌人的直接视线之外。 飞机导弹配备了以高氯酸铵和高氯酸铵为基础的燃料,火箭,手榴弹和带有弹道燃料的反坦克导弹。
火箭燃料能源
为了比较不同类型火箭燃料的能量容量,必须为它们设置可比较的燃烧条件,包括燃烧室中的压力和火箭发动机喷嘴的膨胀程度-例如150大气和300倍膨胀。 然后,对于燃料对/三元组,特定冲量为:
氧气+氢气-4,4 km / s;
氧气+煤油-3,4 km / s;
AT + UDMH-3,3 km / s;
二硝酰胺铵+氢化氢+ octogen-3,2 km / s;
高氯酸铵+铝+ octogen-3,1 km / s;
高氯酸铵+ octogen-2,9 km / s;
硝酸纤维素+硝酸甘油-2,5 km / s
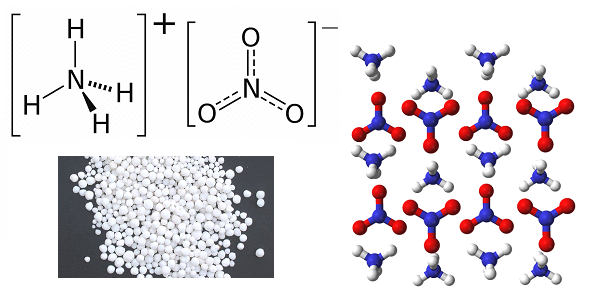
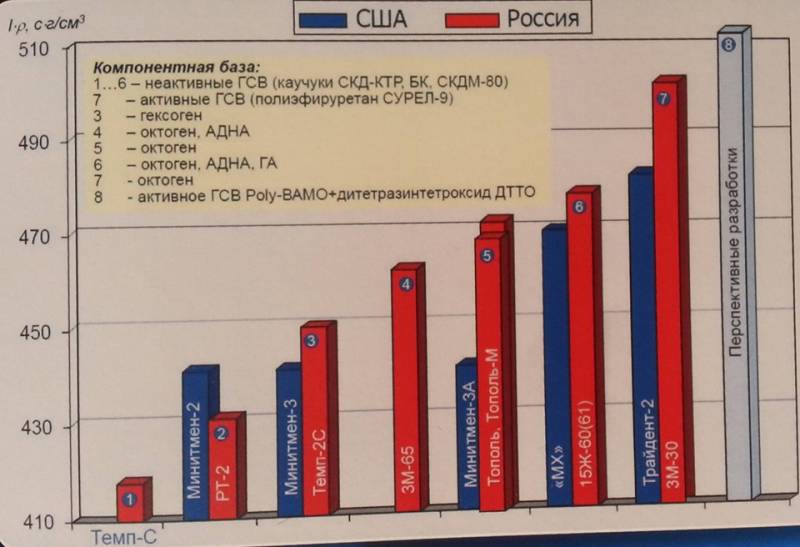
基于二硝酰胺铵的固体燃料是1980-ies晚期的国内开发产品,曾被用作RT-23 UTTX和P-39火箭的第二和第三阶段的燃料,其能量性能仍未被基于高氯酸铵的最佳外国燃料样品所超越,用于Minuteman-3和Trident-2导弹。 二硝酰胺铵是一种炸药,即使在光辐射下也会爆炸;因此,它是在低功率红光灯照亮的房间内产生的。 由于技术上的困难,除苏联以外,世界上任何地方都无法掌握以此为基础的火箭燃料的制造过程。 另一件事是,苏联技术仅在位于乌克兰SSR第聂伯罗彼得罗夫斯克州的Pavlograd化工厂例行实施,而在该工厂改型为生产日用化工品之后的1990年中,这种技术就消失了。 但是,从有前途的RS-26“边境”型武器的战术和技术特征来看,俄罗斯在2010-s中恢复了该技术。
高效成分的一个例子是来自联邦国家统一企业彼尔姆工厂拥有的俄罗斯专利2241693的固体火箭燃料成分 SM 基洛夫“:
氧化剂为二硝胺铵,58%。
燃料-氢化铝,27%;
增塑剂-三硝酸硝基异丁酯甘油,11,25%;
粘合剂-聚丁二烯丁腈橡胶,2,25%;
硬化剂-硫,1,49%;
燃烧稳定剂-超细铝,0,01%;
添加剂-烟灰,卵磷脂等
火箭燃料的发展前景
液体火箭燃料发展的主要领域是(按优先顺序排列):
-使用过冷的氧气以增加氧化剂的密度;
-过渡到氧气+甲烷的燃料对,因为铝制储罐在液态甲烷的温度下进行了硬化,其可燃成分的能量比煤油高15%,热容量比煤油好6倍;
-以24%的含量向氧气中添加臭氧,以增加氧化剂的沸点和能量(大部分臭氧具有爆炸性);
-使用触变(增稠)燃料,其成分包含五硼烷,五氟化物,金属或其氢化物的悬浮液。
Falcon 9运载火箭已经使用过冷氧气;俄罗斯和美国正在开发氧气+甲烷燃料油火箭发动机。
固体火箭燃料的主要发展方向是过渡到分子中含氧的活性粘合剂,从而改善了整体固体燃料的氧化平衡。 这种粘合剂的现代国内实例是Nika-M聚合物组合物,其包括由国家晶体研究所(Dzerzhinsk)开发的二氧化二腈和丁二醇聚醚氨基甲酸酯的环状基团。
另一个有希望的领域是所用硝胺炸药范围的扩大,与八聚体(负22%)相比,它们具有更大的氧平衡。 首先,它是六硝基六氮杂异纤锌矿型结构烷烃(Cl-20,氧平衡为负10%)和八硝基古巴(氧平衡为零),其使用前景取决于降低其生产成本-目前Cl-20比八聚体贵得多,八硝基古巴比Cl高得多-20。
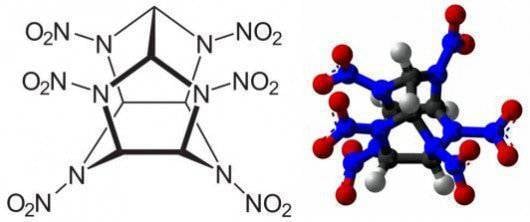
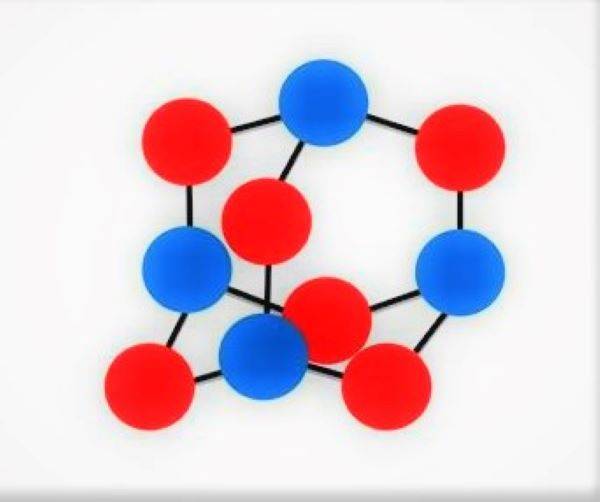
除了改善已知类型的组分外,还朝着产生高分子化合物的方向进行研究,这些高分子化合物的分子仅由通过单键相互连接的氮原子组成。 由于高分子化合物在加热作用下的分解,氮形成通过三键连接的两个原子的简单分子。 在这种情况下释放的能量是硝胺炸药能量的两倍。 在2009百万压力和1°C温度的影响下,俄罗斯和德国科学家在联合实验装置上进行的实验中,俄罗斯和德国科学家首次获得了具有类金刚石晶格的氮化合物。 当前,正在努力实现在常压和常温下氮聚合物的亚稳态。
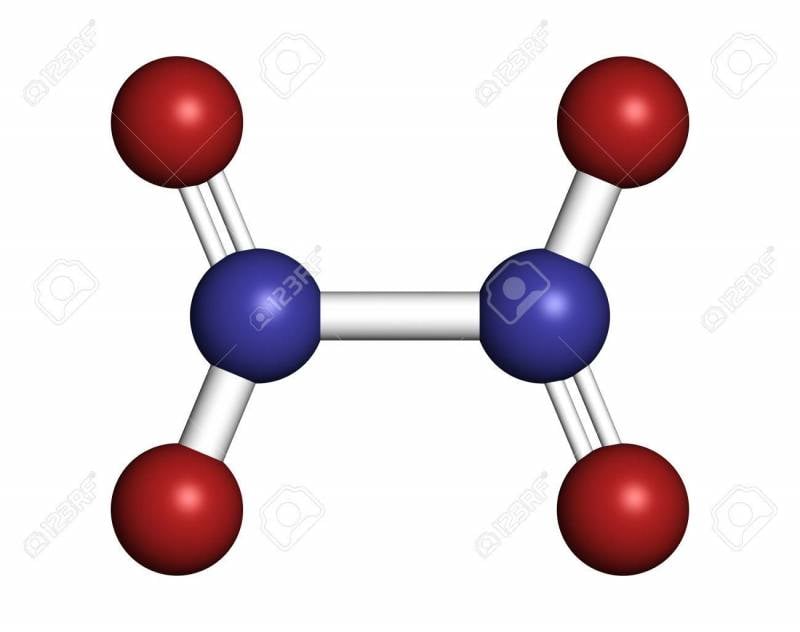
有希望的含氧化合物是较高的氮氧化物。 已知的一氧化氮V(其平面分子由两个氮原子和五个氧原子组成)由于其低熔点(32°C)而不能作为实用的固体燃料组分。 通过寻找合成一氧化氮VI(四氮杂己六氧化物)的方法来进行这一方向的研究,该方法的骨架分子为四面体形式,在其顶部有四个氮原子与位于四面体边缘的六个氧原子键合。 一氧化氮VI分子中原子间键的完全闭合,使得可以预测与urotropine相似的热稳定性。 一氧化氮VI的氧平衡(加上63%)使您可以显着增加固体高能量成分的固体火箭燃料的比重,例如金属,金属氢化物,硝胺和碳氢化合物。
- 安德烈瓦西里耶夫
- Militaryarms.ru,mirnovogo.ru,dic.academic.ru,findpatent.ru,plesetzk.ru,oko-planet.su,glav.su


信息